PUBMED ОБЗОР: Новые подходы к лечению ишемии сосудов гиалуронидазой
Новейший протокол высокодозного импульсного введения гиалуронидазы был разработан Клаудио Делоренци в 2017 году.
Д-р ДеЛоренци является медицинским директором Allergan Canada (Маркхэм, Онтарио, Канада) и Merz Canada (Берлингтон, Онтарио, Канада), а также членом Консультативного совета Kythera Biopharmacueticals Inc. (Вестлейк-Виллидж, Калифорния, США), Suneva Medical Inc. ( Сан-Диего, Калифорния, США) и Valeant Pharmaceuticals (Лаваль, Квебек, Канада).
Основа методики заключается в том, что количество МЕ введенной гиалуронидазы должно зависеть от количества пораженных тканей (т.е. одна доза не подходит всем).
Предполагается, что фермент должен использоваться в концентрации достаточной для обильного промывания закупоренных сосудов и быстрого гидролиза филлер, вызвавшего закупорку. Ишемизированный сосуд, должен быть омыт достаточной концентрацией гиалуронидазы, чтобы диффундировать через артериальную стенку, а затем расщепить ГК на продукты метаболизма, достаточно мелкие, чтобы пройти через капиллярную систему.
Исходя из того, что мы не знаем, какой именно сосуд закупорен, врач должен предполагать, что все сосуды в зоне ишемии закупорены. С этой точки зрения, введение недостаточного количества гиалуронидазы, может привести к частичному распаду эмбола, который будет препятствовать полноценному кровотоку.
Также может случиться, что артериальное давление вытолкнет эмбол ниже по течению кровотока, что приведет к новым участкам ишемии. Фактически возникает феномен «отсроченной» ишемии, когда при продвижении части филлера вниз по кровотоку, он рано или поздно снова перекроет какой-либо сосуд. Поэтому необходим постоянный мониторинг состояния пациента
Целью лечения окклюзии является полное растворение вызывающего обструкцию наполнителя. Для этого необходима достаточная концентрация гиалуронидазы в нужном месте достаточно долго, чтобы привести к (достаточно) полному гидролизу. Количество повторов является преднамеренным, поскольку недостаток любого из этих элементов является препятствием к достижению заявленной цели.
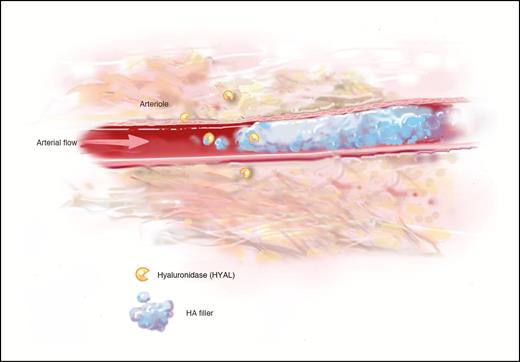
Рисунок 1. Гиалуронидаза диффундирует через артериальную стенку с некоторой скоростью, зависящей от концентрации. Низкие концентрации гораздо менее эффективны клинически. Кажется вероятным, что высокие концентрации гиалуронидазы могут привести к более высоким внутриартериальным концентрациям и, следовательно, к более эффективному гидролизу ГК.
In vitro время отклика на гидролиз зависит от тестируемого наполнителя. Предположим, что для разрушения филлера потребуется, грубо говоря, несколько часов, поскольку гиалуронидаза должна диффундировать через неповрежденную артериальную стенку и гидролизовать наполнитель. (Сшитые наполнители разлагаются дольше под действием фермента, в то время как, в испытаниях автора in vitro несшитая ГК гидролизовалась почти мгновенно, с полным разжижением всего за несколько секунд прямого контакта).
Известно, что сам фермент активно метаболизируется в организме человека, поэтому и он дезактивируется с определенной скоростью, как только его вводят. По мере накопления жидкости из капилляров в ишемической среде концентрация гиалуронидазы падает. Наконец, мы знаем, что по мере того, как фермент разлагает основное вещество, он начинает диффундировать от исходного места инъекции.
Таким образом, мы можем видеть, что количество гиалуронидазы, которое мы первоначально ввели в область, будет частично деактивировано (естественными анти-HYAL агентами), разбавлено жидкостями и физически диффундирует из области, где мы хотим поддерживать высокую концентрацию.
Все эти три фактора снижают действие фермента, и автор предполагает, что именно поэтому, мы должны чаще инъецировать галуронидазу для поддержания высокой концентрации.
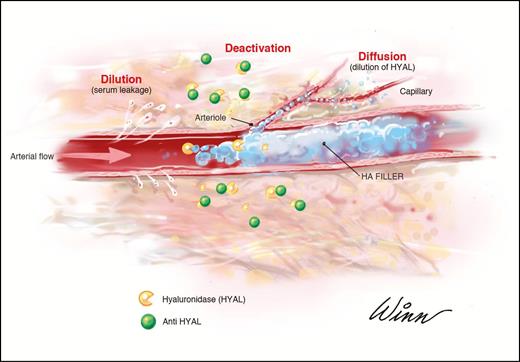
Рисунок 2. Как только гиалуронидаза вводится в ткани, ее концентрация снижается за счет нескольких параллельных процессов. Сыворотка просачивается в ишемизированные ткани, разбавляя фермент, также он постепенно подвергается гидролизу. Одновременно происходит диффузия, снижающая локальную концентрацию.
Частоту дополнительных инъекций необходимо определять в лабораторных исследованиях, но на данный момент автор использует почасовой график дозирования. С клинической точки зрения это кажется безопасным и эффективным, но это может быть чрезмерным, и необходимы исследования диапазона доз на проверенной модели.
Другими возражениями против такого метода, являются туманные опасения по поводу разрушения ГК в окружающих тканях, чем может быть вызван ее хронический дефицит. Несмотря на то, что такого не наблюдалось в реальных клинических случаях, существует два исключения.
Во-первых, длительная ишемия может вызвать гибель клеток (в частности, жировых клеток), поэтому ее неправильно лечение приводит, вероятно, к необратимой атрофии подкожного жира и вторичной атрофии дермы.
Второй пример – лечение инфекции, особенно клинического абсцесса. Это единственный случай, когда автор видит вероятность появления хронического дефицита тканей, т.е. именно недолеченная ишемия или ее неправильное лечение приводит к хронической инфекции с абсцессом. Когда абсцесс гноится в течение определенного периода времени без разреза и дренирования, возникающее в результате воспаление приводит к атрофии подкожного жира, когда жировые клетки как невинные свидетели погибают случайно. Если бы абсцесс был своевременно диагностирован и вылечен (если бы из тканей был удален какой-либо оставшийся резервуар инвазивного организма), дефицита тканей никогда бы не возникло.
В обеих ситуациях мы видим, что в дефиците тканей незаслуженно обвиняют гиалуронидазу, тогда вина полностью лежит на плечах неадекватности клинического лечения.
Нет никаких сомнений в том, что фермент гиалуронидазы разрушает и натуральную ГК, однако ткани обладают естественной эластичностью и в течение нескольких дней восстанавливают баланс ГК в тканях.
Рассмотрим сосуд, заполненный филлером на основе ГК, который перекрыл весь кровоток. Ткани ишемизируются, в них накапливаются продукты метаболизма, начинается ацидоз. Боль появляется только тогда, когда лидокаин метаболизируется (если филлер вводился вместе с лидокаином).
Давайте начнем лечение с дозы гиалуронидазы. Часть ГК распадается на более мелкие фрагменты, но эти фрагменты все еще слишком велики, чтобы пройти через капилляры, которые имеют размер порядка 5–10 микрон (вспомните, как эритроцитам приходится деформироваться, чтобы пройти через самые узкие капилляры). Со временем гиалуронидаза разбавляется сывороткой, просачивающейся из капилляров, что снижает его эффективность. Кроме того, фермент диффундирует от участков с высокой концентрацией к более низким концентрациям. В то же время, конечно, происходит активный гидролиз самого фермента.
Между тем, огромные молекулы ГК расщепились на несколько более мелкие частицы, поэтому может произойти некоторое смещение эмбола ниже по течению, и зона ишемии несколько меняется. Однако, когда концентрация гиалуронидазы падает ниже критического уровня, дальнейшая деградация ГК происходит при гораздо более низкой скорости распада, и обструкция вновь стабилизируется (до тех пор, пока не будет введено больше фирмента).
Мы знаем, что требуется несколько часов, чтобы разрушить некоторые современные филлеры на основе ГК до размера, когда они смогут пройти через капиллярное русло. Крайне важно, поддерживать высокую концентрацию гиалуронидаза, чтобы обеспечить более высокую скорость деградации. Таким образом, нужно продолжать добавлять больше фермента в зону ишемии, чтобы поддерживать деградацию ГК и восстановить в ней нормальный кровоток.
Типичные почасовые дозы гиалуронидазы, применяемые при ишемических повреждениях различного размера, показаны на рис.3.
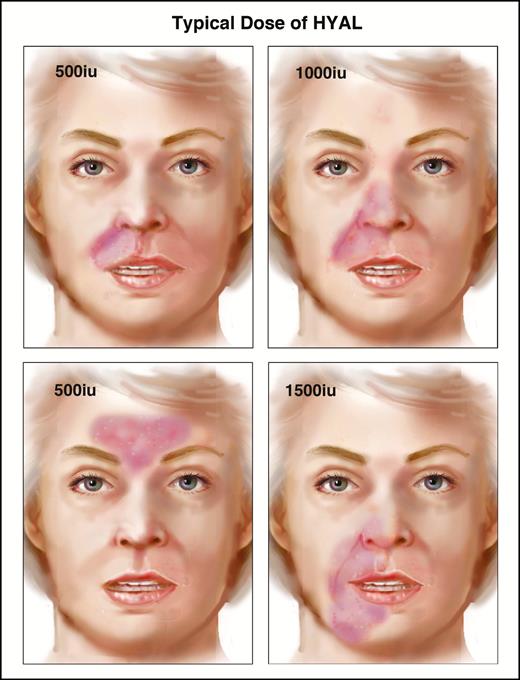
Рисунок 3. Некоторые общие модели травм и типичные дозы, используемые автором для каждой из них. Гиалуронидаза вводится в ишемизированные ткани, а затем используется легкий массаж, чтобы максимизировать время контакта между ишемизированными тканями и ферментом. Ткани могут быть отечными, но легкий массаж после инъекции гиалуронидазы уменьшит отек. Массаж важен для обеспечения максимального контакта между гиалуронидазой и наполнителем, вызывающим непроходимость.
В каком-то смысле это похоже на попытку наполнить протекающий контейнер, поскольку нам нужно поддерживать постоянный уровень гиалуронидазы, тогда как он уменьшается за счет разбавления, диффузии и дезактивации.
НИЗКИЕ ОБЪЕМЫ (LVE) ПРОТИВ ВЫСОКИХ ОБЪЕМОВ (HVE)
Автор определяет эмболию малого объема (LVE) как эмболы, состоящие из 0,1 мл филлера ГК или менее. Это наиболее распространенные типы случайных внутрисосудистых инъекций, с которыми действительно сталкиваются опытные косметологи.
Сосудистые эмболии большого объема (HVE) состоят из эмболов более 0,1 мл. HVE чаще ассоциируется с худшим прогнозом и повреждениями нескольких систем, такими как потеря зрения, потеря слуха или даже инсульт.
Тем не менее, иногда можно встретить HVE, когда половина кубического сантиметра или более была введена в виде болюса непосредственно в артерию.
Большие эмболы априори труднее лечить. Больший объем филлера требует более длительного периода гидролиза, а поддержание достаточно высокой концентрации гиалуронидазы в течение длительного периода времени в большом объеме ткани представляет серьезную проблему.
В центральной части лица, особенно в носу и глабелле, где средний внутриартериальный объем надглазничных, надблоковых и дорсальной носовой артерий приближается к 0,1 мл, становится очевидным, что большой болюс HVE может легко заполнить не только их, но и глазную артерию, а также другие более проксимальные внутричерепные артерии. При коррекции в области виска были случаи, когда эмбол по передней ветви поверхностной височной артерии попадал назад, например, к среднему мозгу, что затем влияло на слух, а также вызывало эмболический инсульт.
ВНУТРИАРТЕРИАЛЬНОЕ ВВЕДЕНИЕ ГИАЛУРОНИДАЗЫ ПРОТИВ ПЕРИВАСКУЛЯРНОГО
HVE включает большие болюсные инъекции в артериальную систему, и они обычно требуют более интенсивного лечения гиалуронидазой, поскольку зона ишемии больше, а растворение эмбола занимает больше времени. В связи с этим встает вопрос, не эффективнее ли будет ввести гиалуронидазу внутриартериально? При тяжелой обструкции, кровоток в зоне ишемии нарушается, поэтому введение непосредственно в окклюзированную артерию заставляет фермент гиалуронидазы отклоняться от зоны ишемии. При периваскулярном введении в самой зоне обструкции, гиалуронидаза благодаря диффундированию разрушает ГК на всем протяжении сосудистого пути, воздействуя сразу на весь эмбол.
Однако эта гипотеза не была проверена, и еще предстоит доказать, является ли периваскулярное введения фермента более или менее эффективным, чем внутриартериальное.
Но, стоит отметить, что на международных встречах были зарегистрированы спорадические случаи неудачного лечения при внутриартериальном применении гиалуронидазы. Это влечет за собой дальнейшую необходимость катетеризации артерии, либо процедуры артериографии, которые обычно недоступны в обычных кабинетах косметолого.
На данный момент, простое периваскулярное введение гиалуронидазы в пораженные участки представляется безопасным и эффективным решением в большинстве случаев. Клинический опыт за последние несколько лет показал, что использование такого метода лечения ишемии дало превосходные результаты.
МЕХАНИЗМ ИНЪЕКЦИИ: КАК ФИЛЛЕР ПОПАДАЕТ В АРТЕРИЮ?
Возможно, что большинство этих событий являются результатом прямой внутриартериальной инъекции с открытием иглы или канюли непосредственно в просвете сосуда. Очевидно, что аспирация перед инъекцией может обеспечить хорошую обратную связь, если видна ярко-красная кровь, но отрицательный результат может ввести в заблуждение.
В областях с рубцовыми тканями, например, в результате предыдущей травмы или даже в результате длительного лечения наполнителями, могут быть особенности.
Когда игла или канюля вводятся в ткани, это создает искусственный путь для потока филлера. Метод, называемый линейно-ретроградных, при котором игла или канюля вводится через ткани, а филлер медленно вводится при их извлечении. Если ткани рубцовые, то игольный канал действует как канал для поступления филлера (рис. 4).
Становится очевидным возможный механизм эмболии. Если в сосуд проникла игла или канюля, даже если наполнитель находится на некотором расстоянии от сосуда, наполнитель может вернуться назад по пути иглы, а затем попасть прямо в сосуд, следуя по пути наименьшего сопротивления.
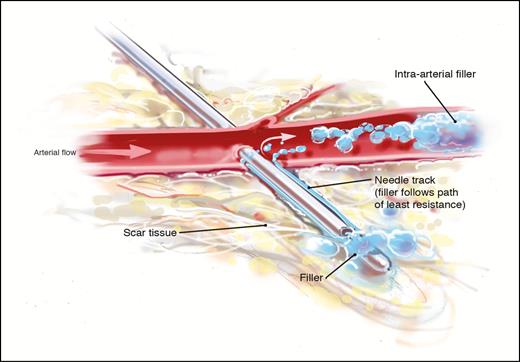
Рисунок 4. Как проникновение в сосуд может вызвать внутрисосудистую эмболию, даже если кончик канюли или иглы находится далеко за просветом сосуда? Предполагается, что это более вероятно, когда в мягких тканях присутствует рубцовая ткань. Проникновение иглы или канюли в рубцовую ткань создает путь для поступления филлера. Данная проблема может стать более распространенной у постоянных пациентов косметолога поскольку каждая процедура введения наполнителя вызывает небольшое количество рубцов в мягких тканях.
Было выдвинуто три конкурирующих гипотезы (табл. 1) относительно патофизиологии, связанной с ишемией.

Сосудистая компрессия связана с идеей, что высокое давление, примыкающее к артерии, может сдавливать ее, аналогично тому, как если бы вы наступили на садовый шланг во время полива цветов.
Сосудистый спазм связан с сокращением мышечных слоев стенок кровеносных сосудов в ответ на химические раздражители (например, табачные изделия; обратите внимание, что сосудистый спазм приводит к атрофии кожи у восприимчивых пациентов в ответ на низкие температуры, механическое раздражение, или воспалительные васкулопатии).
Как правило, химические вещества или лекарства, которые могут вызвать значительный сосудистый спазм, являются вредными, а ГК совсем не вредна (на самом деле, ГК была выбрана в значительной степени потому, что она довольно безвредна и маловероятна для раздражения тканей). Механическое раздражение или стимуляция кровеносного сосуда иногда может вызвать его спазм, но это, как правило, временное состояние, и только в определенных исключительных обстоятельствах (например, хирургическая пересадка) на это важно обращать внимание.
То, что мы имеем дело с острой сосудистой эмболией, подтверждается несколькими линиями доказательств. Во-первых, мы знаем, что в лабораторных условиях у животных в нескольких исследованиях ученые не смогли получить сосудистую недостаточность путем внешней компрессии. Во-вторых, самые прямые доказательства видны при гистологическом исследовании ишемизированной ткани, где мы можем видеть наполнитель в просвете артерий в тканях.
КАК ИЗБЕЖАТЬ ЭМБОЛИИ
Текущая рекомендация клинической практики заключается в том, чтобы вводить объем не более 0,1 мл филлера за один проход в любой области лица, а затем слегка сдвинув кончик иглы сделать инъекцию такого же объема, чтобы, если вы вдруг окажитесь в артерии, в сосуд попадало не более 0,1 мл филлера.
Мы пришли к такому объему много лет назад, оценив размеры небольших артерий в типичных местах инъекций на лице (неопубликованные данные по кадаверному материалу), с той точки зрения, чтобы при попадании врача в одну из них, образовавшийся эмбол не попал во внутреннюю сонную артерию и оттуда в центральную артерию сетчатки. Более свежие данные о надблоковой артерии (как подтверждение данного принципа) показали, что ее средний объем составляет ок. 0,085 мл.
Филлер необходимо вводить под низким давлением, так как высокое давление и высокая скорость потока могут привести к попаданию филлера в нежелательные области.
Наконец, разумно избегать рубцовых тканей и относиться ко всем рубцам как к областям повышенного риска. Наполнитель может течь ретроградно по ходу иглы, а затем проникать в просвет сосуда, поскольку это может быть путь наименьшего сопротивления. Автор отметил неровность тканей у пациентов, длительно применяющих филлеры, и обеспокоен тем, что врачи будут чаще встречать на практике сосудистые эмболии у таких пациентов, поскольку каждое последующее лечение филлерами добавляет немного больше рубцов к тканям.
Обструкция венозного оттока: для большинства областей лица не проблема. В большинстве областей есть избыточные венозные пути, и если один из них заблокирован, соседний легко вступает в игру. Исключениями являются аксиальные или свободные лоскуты, но в них редко, если вообще когда-либо, вводят филлеры.
ВЫСОКОДОЗНОЕ ИМПУЛЬСНОЕ ВВЕДЕНИЕ ГИАЛУРОНИДАЗЫ ДЛЯ LVE
Протокол очень прост, но основан на предположениях автора, которые приведены в таблице 2.
Таблица 2.
Предположения относительно острой ишемии, связанной с введением филлера

Для «одной области» (например, половины верхней губы) сосудистого явления малого объема (LVE, по определению менее 0,1 мл эмбола филлера) доза гиалуронидазы составляет около 450 МЕ. Если нос также поражен, то доза составит 900 МЕ. Доза резко возрастает с размером ишемизированной ткани. Автор утверждает, что по мере увеличения объема ишемизированной ткани должна увеличиваться и дозировка гиалуронидазы, так как целью является достижение минимальной эффективной концентрации HYAL во всем блоке ишемизированной ткани (см. рис. 3).
Мы не знаем точно, где находится закупорка, мы только можем оценить ее клиническую степень по цвету кожи и оценке наполнения капилляров.
Поэтому важно, чтобы по всей области ишемизации была достаточно высокая концентрация HYAL (минимальная эффективная концентрация, какой бы она ни была) во всей зоне. Таким образом, какие бы сосуды ни были заполнены наполнителем ГК по всей ишемизированной ткани, ткани «достаточно пропитываются» гиалуронидазой, чтобы разбить его на компоненты, достаточно мелкие, чтобы пройти через капилляры.
Как только побочные продукты попадут в венозную систему, они, несомненно, будут продолжать расщепляться или отфильтровываться в межальвеолярных перегородках.
В итоге, цель лечения состоит в том, чтобы наполнить ишемизированную ткань достаточным количеством гиалуронидазы для разрушения наполнителя ГК. Поскольку фермент постоянно биодеградирует, мы должны инъецировать его, отсюда и почасовой график дозирования.
ОЦЕНКА ОБЪЕМА ТКАНЕЙ
Автор предполагает, что объем гиалуронидазы должен быть равен примерно 150МЕ на 1 куб. см. Например, половина верхней губы оценивается автором как 3 куб.см (очень грубое приближение, которое, кажется, работает клинически).
Можно попытаться оценить объем вовлеченной в ишемию тканей, а дозу гиалуронидазы увеличивать согласно объему тканей.
При определении того, сколько гиалуронидазы использовать, автор должен оценить объем задействованной в ишемии ткани, т. е. не только площадь поверхности зоны повреждения. Значит, если вовлекаются толстые ткани латеральной стороны щеки ниже скуловой кости радиально к верхним молярам (размер которых составляет около 25 мм по измерениям на кадавере, проведенным автором, т. е. чуть более чем в два раза превышает толщину верхней губы), то необходимо использовать больше гиалуронидазы на единицу площади поверхности по сравнению с верхней губой (размер которой составляет около 12 мм) или надбровной дугой (толщина которой составляет около 6 мм).
Другими словами, врач должен попытаться объективно оценить объем ишемизированной ткани с целью использования достаточной дозы гиалуронидазы, если вовлечены более толстые ткани.
Несмотря на то, что точно оценить объемы тканей «на глаз» невозможно, но даже очень грубые подсчеты необходимой дозы, основанные на размерах тканей, достаточно для успешного лечения.
Автор обращает внимание, что эти цифры получены благодаря его клинической практике, а не в результате каких-либо научных испытаний. Несомненно, эти дозы, будут изменяться в ходе дальнейших исследований.
Правда в том, что никто на самом деле не знает минимальную эффективную дозу гиалуронидазы для использования в терапии. Тем не менее, негативный опыт лечения был очень низким, а положительный эффект был высоким, с полным выздоровлением без осложнений, только за исключением тех случаев, когда начало лечения было отсрочено или, когда использовалось недостаточное количество гиалуронидазы.
Важно внимательно рассматривать каждый случай лечения и корректировать дозу гиалуронидазы согласно объему ишемизированной ткани.
В некоторых случаях, например, область ишемии может затрагивать верхнюю губу и одну сторону носа, а через некоторое время область поражения уменьшается, и охватывает уже только часть исходной зоны, скажем, нос. Таким образом, было бы целесообразно уменьшить дозу гиалуронидазы и повторно обработать область носа.
Возможно, более низкая концентрация гиалуронидазы может быть столь же эффективной. Однако автор утверждает, что более высокие режимы дозирования кажутся клинически безопасными, а результаты лучше, чем при использовании более консервативных дозировок.
ПОСЛЕДСТВИЯ ЭМБОЛИИ ЦЕНТРАЛЬНОЙ АРТЕРИИ СЕТЧАТКИ
Сообщалось, что ретробульбарную инъекцию гиалуронидазы следует рассматривать как лечение эмболии филлерами ГК центральной артерии сетчатки. Тем не менее, клинические обсуждения с врачами, которые действительно пробовали эту технику, не были обнадеживающими (неопубликованные данные), и на сегодняшний день не было опубликовано сообщений об успешном восстановлении зрения у любого из пациента, поступившего без зрительных реакций.
Мы знаем, что экспериментальная окклюзия центральной артерии сетчатки у макак-резусов продемонстрировала строгие временные ограничения, составлявшие около 97 минут до появления необратимых последствий. В строгом смысле существует определенный временной лимит, составляющий около полутора часов от начала потери зрения до восстановления кровообращения. Если восстановление кровообращения задерживается всего на несколько минут сверх этого предела, например, на 105 минут, некоторая степень повреждения у обезьян (и, вероятно, также у людей) остается необратимой.
Учитывая, что гиалуронидаза должна быть подготовлена, введена в ретробульбарное пространство, а затем диффундирована по всему пространству (и до сих пор никто даже не продемонстрировал, что гиалуронидаза может даже диффундировать через склеру), кажется маловероятным, что это лечение будет эффективным.
Этот метод, вероятно, эффективен только в том случае, если сосудистая обструкция возникает во внеглазной части центральной артерии сетчатки (или если обструкция была связана с какой-либо другой частью системы, такой как длинная и короткая цилиарные артерии, или сосуды, поддерживающие зрительный нерв), неясно, будет ли у гиалуронидазы достаточно времени для гидролиза филлера ГК в рамках этих строгих временных ограничений.
К любому времени, необходимому для гидролиза конкретного используемого наполнителя ГК, мы должны добавить время для диффузии гиалуронидазы в эмболы.
Это область, которая, очевидно, требует дальнейших исследований, и, хотя автор не хочет никого отговаривать от использования этой техники, но и чудес ожидать не стоит. Если филлер уже попал в глазное яблоко и обосновался в сетчатке, прогноз, скорее всего, неблагоприятный.
Причины, по которым мы успешно работем с эмболами в коже, заключаются именно в том, что эти ткани довольно устойчивы к длительным приступам ишемии, тогда как сетчатка имеет очень ограниченные и, по-видимому, строгие временные ограничения на ее ишемическую выживаемость.
Техника ретробульбарной инъекции довольно проста в исполнении, и автор был обучен ее технике на кадаверном материале. С помощью иглы 25 g и длиной 1,5 дюйма доступ к орбите осуществляется через латеральную часть нижнего века ниже угла глазной щели. Кончик иглы направляют немного вверх и височно (латерально), а кончик иглы «водят» вдоль латеральной стенки орбиты до тех пор, пока не будет введено от 2/3 до 3/4 длины иглы (около одного дюйма). Затем в этом месте возникает небольшое углубление, после чего можно медленно ввести около 3 см3 гиалуронидазы (всего от 2 до 4 см3).
Внутривенное введение гиалуронидазы при потере зрения: новый терапевтический подход [2]
Несмотря на редкость, увеличение количества сообщений о случаях потери зрения после эстетических инъекций лица вызвало обзоры мировой литературы и создание экспертных групп консенсуса, которые впоследствии создали рецензируемые рекомендации для помощи в неотложной помощи при этом катастрофическом осложнении.
До недавнего исследования Cameron Chestnut (Chestnut C. Restoration of visual loss with retrobulbar hyaluronidase injection after hyaluronic acid filler. Dermatol Surg. 2018;44(3):435–437), подробно описывающего успешное восстановление зрения после ретробульбарной инъекции гиалуронидазы, предыдущие опубликованные попытки терапии эмболизации не увенчались успехом.
Кроме того, был опубликован ряд подходов, альтернативных общепринятым, включая артериальный тромболизис и прямую внутриартериальную инъекцию гиалуронидазы под рентгенологическим контролем, что привело к частичной реканализации артерий; однако это лечение все еще остается недоступным для большинства врачей-косметологов.
В этой части обсуждается внутривенное введение высоких доз гиалуронидазы как относительно безопасный и ранее не изученный подход, который можно использовать, если зрение не было восстановлено, и как альтернативу ретробульбарной инъекции в случае, если опытный офтальмолог не может выполнить эту процедуру в течение 60–90 минут, после чего слепота становится необратимой.
В 1970-х годах гиалуронидаза исследовалась как потенциальное средство для лечения инфаркта миокарда. Неудивительно, что в контексте современного понимания тромбообразования польза при этом состоянии была умеренной; тем не менее, ряд опубликованных исследований демонстрирует безопасное использование гиалуронидазы в этой экстренной ситуации. В некоторых исследованиях дозы 500 МЕ/кг вводились в виде внутривенного болюса, такую же инъекцию повторяли через 6 часов . Период полувыведения из кровотока составляет приблизительно от 2 до 5 минут. Побочные эффекты, связанные с гиалуронидазой, были зарегистрированы как легкие. Случаев анафилаксии не было.
Автор предлагает вводить внутривенно меньшую дозу от 200 до 250 МЕ/кг, если другие стратегии лечения не помогли восстановить зрение после инъекции филлера на основе гиалуроновой кислоты. Для взрослого человека весом 70 кг это примерно 10 ампул гиалуронидазы, имеющейся в продаже порошковой формы гиалуроновой кислоты, в общей дозе 15 000 МЕ. В каждую ампулу вводят 1 мл физиологического раствора для инъекций, пока не будет приготовлена общая болюсная доза 15 000 МЕ в 10 мл физиологического раствора. Вводится внутривенная канюля и вводится болюс с последующей промывкой 10 мл. Пациент остается лежать на спине, а адреналин и кислород доступны в случае анафилаксии.
В течение следующих 5-10 минут, в течение которых гиалуронидаза остается в кровотоке, при среднем объеме крови 5 л мы ожидаем концентрацию гиалуронидазы 3 МЕ на каждый 1 мл циркулирующего объема. Ожидается, что в течение первого или второго сердечного ударного объем гиалуронидаза переместится из венозного в артериальное кровообращение, включая внутреннюю и наружную сонные артерии, затем попадет в лицевую артерию и анастомозирует с артерией сетчатки, способствуя деградации эмбола гиалуроновой кислоты.
Этот непрерывный поток в течение даже 2-3-минутного периода в сочетании с постоянными мерами, такими как возвратное дыхание и массаж орбитальной области, можно считать крайне вероятным результатом реканализации ретинальных или цилиарных артерий.
Достаточная концентрация продукта в просвете окружающего и анастомозного кровообращения в течение более чем нескольких минут делает восстановление зрения высоко вероятным. Кроме того, гиалуронидаза в кровотоке может растворять любые другие артериальные эмболы, в том числе в мозговом артериальном кровообращении, которые, как известно, осложняют примерно 24 процента случаев слепоты.
Внутривенное использование продукта не соответствует протоколу использования фермента гиалуронидазы, также как и ретробульбарная инъекция и любое использование в эстетической медицине, и информированное согласие на лечение с помощью гиалуронидазы должно сопровождаться согласием на лечение филлерами.
Источник:
1. Claudio DeLorenzi. New High Dose Pulsed Hyaluronidase Protocol for Hyaluronic Acid Filler Vascular Adverse Events. Aesthetic Surgery Journal, Volume 37, Issue 7, July-August 2017, Pages 814–825, https://doi.org/10.1093/asj/sjw251
2. Mccann M. Intravenous Hyaluronidase for Visual Loss Secondary to Filler Injection: A Novel Therapeutic Approach. The Journal of Clinical and Aesthetic Dermatology. 2019 Dec;12(12):25-27. PMID: 32038761; PMCID: PMC7002050.
прочитано
14711
раз